Questões resolvidas de vestibulares sobre radioatividade, fusão e fissão nuclear, raios alfa, beta e gama
1) (ENEM) Um problema ainda não resolvido da geração nuclear de eletricidade é a destinação dos rejeitos radiativos, o chamado “lixo atômico”. Os rejeitos mais ativos ficam por um período em piscinas de aço inoxidável nas próprias usinas antes de ser, como os demais rejeitos, acondicionados em tambores que são dispostos em áreas cercadas ou encerrados em depósitos subterrâneos secos, como antigas minas de sal. A complexidade do problema do lixo atômico, comparativamente a outros lixos com substâncias tóxicas, se deve ao fato de
1) (ENEM) Um problema ainda não resolvido da geração nuclear de eletricidade é a destinação dos rejeitos radiativos, o chamado “lixo atômico”. Os rejeitos mais ativos ficam por um período em piscinas de aço inoxidável nas próprias usinas antes de ser, como os demais rejeitos, acondicionados em tambores que são dispostos em áreas cercadas ou encerrados em depósitos subterrâneos secos, como antigas minas de sal. A complexidade do problema do lixo atômico, comparativamente a outros lixos com substâncias tóxicas, se deve ao fato de
a) emitir radiações nocivas, por milhares de anos, em um processo que não tem como ser interrompido artificialmente.
b) acumular-se em quantidades bem maiores do que o lixo industrial convencional, faltando assim locais para reunir tanto material.
c) ser constituído de materiais orgânicos que podem contaminar muitas espécies vivas, incluindo os próprios seres humanos.
d) exalar continuamente gases venenosos, que tornariam o ar irrespirável por milhares de anos.
e) emitir radiações e gases que podem destruir a camada de ozônio e agravar o efeito estufa.
2) (FUVEST) Medidas de radioatividade de uma amostra de tecido vegetal encontrado nas proximidades do Vale dos Reis, no Egito, revelaram que o teor em carbono 14 (a relação 14C/12C) era correspondente a 25% do valor encontrado para um vegetal vivo. Sabendo que a meia-vida do carbono 14 é 5730 anos, conclui-se que o tecido fossilizado encontrado não pode ter pertencido a uma planta que viveu durante o antigo império egípcio – há cerca de 6000 anos -, pois:
A) a meia-vida do carbono 14 é cerca de 1000 anos menor do que os 6000 anos do império egípcio.
B) para que fosse alcançada esta relação 14C/12C no tecido vegetal, seriam necessários, apenas, cerca de 3000 anos.
C) a relação 14C/12C de 25%, em comparação com a de um tecido vegetal vivo, corresponde à passagem de, aproximadamente, 1500 anos.
D) ele pertenceu a um vegetal que morreu há cerca de 11500 anos.
E) ele é relativamente recente, tendo pertencido a uma planta que viveu há apenas 240 anos, aproximadamente.
3) (FMTM) A ciência tem comprovado que o cigarro contém substâncias cancerígenas e que pessoas fumantes apresentam probabilidade muito maior de contrair o câncer quando comparadas com as não fumantes. Além dessas substâncias, o tabaco contém naturalmente o isótopo radioativo polônio de número de massa 210, cujo núcleo decai emitindo uma partícula alfa. O quadro apresenta alguns elementos químicos com os seus respectivos números atômicos.

O núcleo resultante, após o decaimento do polônio 210, é um isótopo do elemento
A) astato
B) bismuto
C) chumbo
D) polônio
E) radônio
4) (UNIUBE - MG) Os valores da massa e carga de uma partícula beta negativa (b-) indicam que esta é idêntica ao:
a) átomo de hidrogênio
b) átomo de hélio
c) próton
d) nêutron
e) elétron
5) (FEI) A bomba de hidrogênio é um exemplo de reação nuclear:
a) do tipo fissão;
b) onde ocorre apenas emissão de raios alfa;
c) onde ocorre apenas emissão de raios beta;
d) do tipo fusão;
e) onde ocorre apenas emissão de raios gama.
Quando um elemento radioativo emite um raio:
a) a, seu número atômico diminui de duas unidades;
b) b, seu número atômico aumenta de uma unidade;
c) g, ocorre emissão de onda eletromagnética;
d) a, seu número atômico diminui de quatro unidades;
e) b, seu número atômico aumenta de duas unidades;
a) do tipo fissão;
b) onde ocorre apenas emissão de raios alfa;
c) onde ocorre apenas emissão de raios beta;
d) do tipo fusão;
e) onde ocorre apenas emissão de raios gama.
6) (MACK) Assinale a alternativa incorreta.
Quando um elemento radioativo emite um raio:
a) a, seu número atômico diminui de duas unidades;
b) b, seu número atômico aumenta de uma unidade;
c) g, ocorre emissão de onda eletromagnética;
d) a, seu número atômico diminui de quatro unidades;
e) b, seu número atômico aumenta de duas unidades;
7) (UnB) Os raios catódicos são:
a) constituídos de prótons
b) constituídos de elétrons
c) constituídos de nêutrons
d) constituídos de prótons, nêutrons e elétrons
d) n.d.a.
a) constituídos de prótons
b) constituídos de elétrons
c) constituídos de nêutrons
d) constituídos de prótons, nêutrons e elétrons
d) n.d.a.
8) Quando nêutrons atingem núcleos de átomos de nitrogênio com número de massa 14, há formação de átomos de carbono com o mesmo número de massa que o dos núcleos bombardeados. Qual a equação nuclear completa dessa reação?
Nos atômicos: C = 6, N = 7
Nos atômicos: C = 6, N = 7
9) A Mecânica Quântica explica ou permite previsões de todas, exceto de uma das seguintes características dos átomos. Identifique a exceção:
a) a probabilidade de um elétron estar em uma dada região em certo instante.
b) os níveis de energia que o elétron pode ocupar.
c) a simetria geral dos orbitais eletrônicos.
d) as freqüências de luz absorvidas ou emitidas por átomos gasosos.
e) o caminho ou trajetória dos elétrons.
a) a probabilidade de um elétron estar em uma dada região em certo instante.
b) os níveis de energia que o elétron pode ocupar.
c) a simetria geral dos orbitais eletrônicos.
d) as freqüências de luz absorvidas ou emitidas por átomos gasosos.
e) o caminho ou trajetória dos elétrons.
10) (UFBA) Os raios T, produzidos nas explosões solares, vibram mais lentamente que os raios gama e têm alta intensidade. Esses fatos os colocam como fortes candidatos para a leitura de imagens médicas já que oferecem menor risco para os pacientes. Acredita-se que a radiação na faixa dos Terahertz seja produzida por partículas atômicas eletricamente carregadas, aceleradas a velocidades próximas à da luz — 3,0.108 m/s. Curiosamente, essa forma de radiação surge também em experimentos feitos em aceleradores de partículas, equipamentos usados em testes de física atômica. (OS NOVOS raios de sol. In: Pesquisa FAPESP, 2004, p.45).
 Cu
Cu 
 Zn +
Zn +
Características e comportamento das partículas eletrizadas e suas interações nos sistemas vivos podem ser expressas nas seguintes proposições:
(01) A energia luminosa é convertida em energia química nas moléculas de glicose, em processo próprio dos fotoautótrofos, dependente de propriedades da clorofila.
(02) O uso da água como doador de hidrogênio na fotossíntese propiciou a expansão da vida aeróbica.
(04) A noção de partículas atômicas eletricamente carregadas surge nas Ciências Naturais somente após a proposição de um modelo atômico por J. Thomson.
(08) A partícula de carga q e massa m acelerada exclusivamente por um campo magnético uniforme e perpendicular à sua velocidade realiza um movimento de período igual a  .
.
 .
.
(16) As partículas carregadas que se deslocam sem deflexão, em uma região do selecionador de velocidades onde existe um campo magnético uniforme  e um campo elétrico uniforme
e um campo elétrico uniforme 
ortogonais entre si, têm velocidade de módulo igual a .
.
 e um campo elétrico uniforme
e um campo elétrico uniforme 
ortogonais entre si, têm velocidade de módulo igual a
 .
.
11) (FUVEST) O isótopo radioativo Cu-64 sofre decaimento , conforme representado:
 Cu
Cu 
 Zn +
Zn +
A partir de amostra de 20,0 mg de Cu-64, observa-se que, após 39 horas, formaram-se 17,5mg de Zn-64. Sendo assim, o tempo necessário para que metade da massa inicial de Cu-64 sofra decaimento é cerca de
a) 6 horas.
b) 13 horas.
c) 19 horas.
d) 26 horas.
e) 52 horas.
Observação:  Cu
Cu
 Cu
Cu
64 = número de massa
29 = número atômico
12) (PUC-RIO 2007) Considere a equação nuclear incompleta:

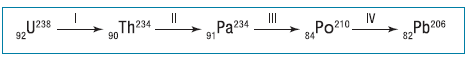





60) (UEL-2003) A Usina Nuclear de Angra dos Reis - Angra II - está projetada para uma potência de 1309 MW. Apesar de sua complexidade tecnológica, é relativamente simples compreender o princípio de funcionamento de uma usina nuclear, pois ele é similar ao de uma usina térmica convencional. Sobre o assunto, considere as afirmativas apresentadas a seguir.
I. Na usina térmica, o calor gerado pela combustão do carvão, do óleo ou do gás vaporiza a água em uma caldeira. Esse vapor aciona uma turbina acoplada a um gerador e este produz eletricidade.
II. O processo de fusão nuclear utilizado em algumas usinas nucleares é semelhante ao processo da fissão nuclear. A diferença entre os dois está na elevada temperatura para fundir o átomo de Urânio-235.
III. Na usina nuclear, o calor é produzido pela fissão do átomo do Urânio-235 por um nêutron no núcleo do reator.
IV. Na usina nuclear, o calor é produzido pela reação em cadeia da fusão do átomo do Urânio-235 com um nêutron.
São corretas apenas as afirmativas:
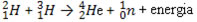 Portanto, podemos afirmar que:
Portanto, podemos afirmar que:
Cálculo de b: 7 + 0 = 6 + b \ b = 1
1y1 = 1p1 (próton)
A equação completa é: 7N14 + 0n1 - 6C14 + 1p1
Para completar a equação, é correto afirmar que o amerício-240 é um isótopo radioativo que se obtém, juntamente com um próton e dois nêutrons, a partir do bombardeio do plutônio-239 com:
A) partículas alfa.
B) partículas beta.
C) radiações gama.
D) raios X.
E) deutério.
13) (UFRJ) A sequência simplificada abaixo mostra as etapas do decaimento radioativo do isótopo urânio-238:
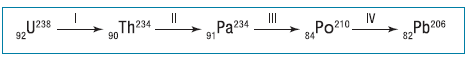
Determine o número de partículas 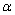 e ß emitidas na etapa III e identifique, por seus símbolos, os átomos isóbaros presentes na sequência.
e ß emitidas na etapa III e identifique, por seus símbolos, os átomos isóbaros presentes na sequência.
14) (UFV/2011) Vários elementos pesados como o urânio e o rádio sofrem desintegração radioativa. Ao emitirem uma partícula alfa
são convertidos, respectivamente, em:
15) Uma amostra de 10 g de água de rio mostrou conter 8.10-18 átomos de trítio (H – 3) por átomo de hidrogênio comum (H – 1). O trítio se decompõe radioativamente com meia-vida de 12,26 anos. Quantos átomos de trítio restarão após 40 anos se a amostra for conservada intacta?
16) (IME) Os isótopos do urânio U-238 e U-235 aparecem na natureza sempre juntos. Como o U-235 não é gerado a partir do U-238 por desintegração e admitindo que não há razão para privilegiar um em relação ao outro, podemos supor que o Criador os tenha colocado em proporções iguais no momento da formação da Terra. Considerando válida tal hipótese, calcule a idade que nosso planeta teria.
Dados:
Tempo de meia – vida do U-238 : 4,50 .109 anos
Tempo de meia – vida do U-235 : 7,07 .108 anos
Abundância isotópica do U-238 : 99,28%
Abundância isotópica do U-235 : 0,72%
Tempo de meia – vida do U-235 : 7,07 .108 anos
Abundância isotópica do U-238 : 99,28%
Abundância isotópica do U-235 : 0,72%
17) Que volume de hélio nas CNTP (em mL) será produzido em um ano a partir de um grama de Po-210? O Po-210 é um alfa emissor de meia vida de 138,40 dias.
18) (IME) O decaimento do núcleo de Na-24 que possui meia-vida de 15 horas, dá-se por emissão de partículas β, produzindo o isótopo estável Mg-24. Partindo de 200 mg de Na-24, determine o tempo necessário para que a relação entre as massas dos isótopos de Mg e Na seja de 1 para 3.
Ddos: log2 = 0,3
log3 = 0,47
19) (UERJ) O isótopo rádio-226, utilizado em tratamentos medicinais, é um alfa-emissor com tempo de meia-vida de 3,8 dias.Para estudar a decomposição do rádio-226, realizou-se um experimento em que uma amostra sólida de 1 mol dessa substância foi introduzida em uma ampola com capacidade de 8,2 L.
Nessa ampola, a pressão interna inicial era igual a 1,5 atm e a temperatura, constante em todo o experimento, igual a 27 °C. Considere as informações abaixo:
- o decaimento do rádio-226 produz radônio-222 e hélio-4;
- os gases hélio e radônio têm comportamento ideal;
- não há reação entre os gases no interior da ampola.
Calcule a pressão, em atm, no interior da ampola, 7,6 dias após o início do experimento.
20) (ITA-SP) Um dos isótopos do einstênio, 99Es-253, quando bombardeado com partículas alfa, forma um isótopo do elemento X e 2 nêutrons. Determine os números atômico e de massa desse isótopo.
Comum às questões: 21 e 22
Cobalto-60, radioisótopo utilizado na terapia do câncer, é obtido em reatores nucleares a partir do isótopo natural cobalto-59, não radioativo. Esse radioisótopo, cuja meia-vida é de, aproximadamente, 5 anos, emite radiação  , acompanhada de radiação
, acompanhada de radiação  de alta energia.
de alta energia.
21) (UNINOVE SP) Uma cápsula, recém-preparada, contendo o radioisótopo em questão terá sua atividade radioativa reduzida a cerca de 3% da atividade inicial daqui a, aproximadamente,
a) 5 anos. b) 10 anos. c) 15 anos. d) 20 anos. e) 25 anos.
22) (UNINOVE SP) O isótopo natural cobalto-59 transforma-se no radioisótopo cobalto-60 por captura de X. Ao emitir radiação, esse radioisótopo transforma-se em isótopo do elemento Y.
Esse texto fica correto quando X e Y são substituídos, respectivamente, por
a) próton e níquel. b) próton e ferro. c) elétron e ferro. d) nêutron e níquel. e) nêutron e ferro.
23) No acidente nuclear de Chernobyl, a falha no sistema de refrigeração resultou no aquecimento que deu origem à explosão seguida de incêndio de grandes blocos de grafite, lançando no ar 6 a 7 toneladas de material radioativo. A alternativa usada para controlar o processo foi o aterramento do reator com toneladas de areia e concreto.
Indique a alternativa correta:
a) O 92U235 decai com emissão de 7 partículas alfa e quatro partículas beta para produzir 82Pb206.
b) os efeitos sobre o meio ambiente pela liberação do isótopo Cs137 ( meia-vida 30 anos) deverão ser detectados até 30 anos após o acidente.
c) a energia gerada em usinas nucleares se origina de um processo de fusão nuclear.
d) a fissão do 92U235 se dá por um processo de reação em cadeia.
e) blocos de grafite funcionam como aceleradores, aumentando a velocidade dos nêutrons.
24) (UNIFESP SP) Mais de uma vez a imprensa noticiou a obtenção da chamada fusão nuclear a frio, fato que não foi comprovado de forma inequívoca até o momento. Por exemplo, em 1989, Fleishman e Pons anunciaram ter obtido a fusão de dois átomos de deutério formando átomos de He, de número de massa 3, em condições ambientais. O esquema mostra, de forma simplificada e adaptada, a experiência feita pelos pesquisadores.

Uma fonte de tensão (por exemplo, uma bateria de carro) é ligada a um eletrodo de platina e a outro de paládio, colocados dentro de um recipiente com água pesada (D2O) contendo um eletrólito (para facilitar a passagem da corrente elétrica). Ocorre eletrólise da água, gerando deutério (D2) no eletrodo de paládio. O paládio, devido às suas propriedades especiais, provoca a dissociação do D2 em átomos de deutério, os quais se fundem gerando 3He com emissão de energia.
a) Escreva a equação balanceada que representa a semi-reação que produz D2 no eletrodo de paládio. Explique a diferença existente entre os núcleos de H e D.
b) Escreva a equação balanceada que representa a reação de fusão nuclear descrita no texto e dê uma razão para a importância tecnológica de se conseguir a fusão a frio.
25) (UESC BA) O campo de aplicação da radioatividade é vasto e seu uso pode trazer benefícios para a humanidade, desde que a ética e o bem-estar social sejam prioridade.
Dentre as aplicações da radioatividade, está descrita corretamente a afirmação expressa em
01. Datação de achados arqueológicos usando decaimento de carbono-12.
02. Radioterapia usando raios-X gerados na desintegração do césio -137.
03. Fusão dos radionuclídeos 235U e 238U para gerar energia.
04. Fissão do núcleo de He em núcleos 1H e 2H na bomba de hidrogênio.
05. Síntese de nuclídeos artificiais por transmutação nuclear.
26) duração do efeito de alguns fármacos está relacionada à sua meia-vida, tempo necessário para que a quantidade original do fármaco no organismo se reduza à metade. A cada intervalo de tempo correspondente a uma meia-vida, a quantidade de fármaco existente no organismo no final do intervalo é igual a 50% da quantidade no início desse intervalo.
 O gráfico acima representa, de forma genérica, o que acontece com a quantidade de fármaco no organismo humano ao longo do tempo.
O gráfico acima representa, de forma genérica, o que acontece com a quantidade de fármaco no organismo humano ao longo do tempo.
 O gráfico acima representa, de forma genérica, o que acontece com a quantidade de fármaco no organismo humano ao longo do tempo.
O gráfico acima representa, de forma genérica, o que acontece com a quantidade de fármaco no organismo humano ao longo do tempo.
F. D. Fuchs e Cher l. Wannma. Farmacologia Clínica. Rio de Janeiro: Guanabara Koogan,1992, p. 40.
A meia-vida do antibiótico amoxicilina é de 1 hora. Assim, se uma dose desse antibiótico for injetada às 12 h em um paciente, o percentual dessa dose que restará em seu organismo às 13 h 30 min será aproximadamente de
a) 10%.
b) 15%.
c) 25%.
d) 35%.
e) 50%.
27) (FATEC SP) Uma das características das últimas décadas foram as crises energéticas. Neste contexto, tivemos várias notícias nos jornais relacionadas com diferentes formas de geração de energia. As afirmativas abaixo poderiam ter constado de algumas dessas matérias.
00. O reator nuclear Angra II gera energia através da fusão nuclear de átomos de urânio enriquecido.
01. A queima de combustível fóssil, por exemplo, a gasolina, constitui-se, na realidade, numa reação de oxidação de matéria orgânica.
02. A queima de uma dada quantidade de carvão em uma termoelétrica produz a mesma quantidade de energia que a fissão de igual massa de urânio em uma usina nuclear.
03. A afirmativa anterior (proposição 2-2) está errada, porque a energia liberada numa fissão nuclear é milhões de vezes maior do que a energia liberada na queima (uma reação química) do carvão.
04. Partindo do pressuposto que é possível aproveitar a energia solar para gerar corrente elétrica, utiliza-se a eletrólise da água durante o dia, queimando-se o hidrogênio produzido durante a noite.
28) (UESC BA) Militar defende construção de bomba atômica brasileira, alegando que o Brasil é alvo de cobiça por ter água, alimentos e energia. [...]. “Nós temos de ter, no Brasil, a possibilidade futura de desenvolver um artefato nuclear. Não podemos ficar alheios à realidade do mundo”.
(Correio da Bahia, nov. 2007, p.2, Brasília: ABR).
Dentre outros aspectos que devem ser levados em consideração para que o Brasil possa desenvolver um artefato nuclear, pode-se destacar
01. o bloqueio da reação nuclear de absorção de nêutrons pelo urânio 238 e conseqüente transformação em plutônio 239, após emissão de partículas  .
.
02. o domínio da tecnologia de enriquecimento do urânio natural,  , que possibilita a elevação do percentual de
, que possibilita a elevação do percentual de  até valores de ordem de 90%.
até valores de ordem de 90%.
03. a separação dos gases  e
e  que facilita o processo de purificação do urânio 238 utilizado para a construção da bomba atômica.
que facilita o processo de purificação do urânio 238 utilizado para a construção da bomba atômica.
04. a produção de massas subcríticas de plutônio 239 capazes de produzir a explosão de uma bomba atômica.
05. a inexistência de tecnologia de controle da velocidade de emissão de nêutrons, utilizando-se água pesada, D2O(l), em reatores nucleares.
29) (UFMS) Os raios cósmicos, que são emissões radioativas, bombardeiam nosso planeta, sendo o sol a grande fábrica de partículas radioativas mais próxima de nós. Ele, há milhões de anos, vem emitindo radiações para todo o Universo. Na Terra, isótopos de determinados elementos são também radioativos.
Considerando os radioisótopos e a reação genérica  é correto afirmar que:
é correto afirmar que:
01.  é um metal do bloco d, enquanto
é um metal do bloco d, enquanto  , um não-metal possuindo oito elétrons na camada de valência.
, um não-metal possuindo oito elétrons na camada de valência.
02.  possui 134 nêutrons, enquanto
possui 134 nêutrons, enquanto  possui 142.
possui 142.
04. p é igual a 2, enquanto q é igual a 3.
08. quando  decai a
decai a  , perde 4 prótons e 8 nêutrons.
, perde 4 prótons e 8 nêutrons.
16. quando um radioisótopo só emite uma partícula , há uma diminuição de 2 unidades no seu número atômico e de 4 unidades no seu número de massa.
30) (UFRRJ) Um átomo  emite uma partícula alfa, transformando-se num elemento R, que, por sua vez, emite duas partículas beta, transformado-se num elemento T, que emite uma partícula alfa, transformando-se no elemento D.
emite uma partícula alfa, transformando-se num elemento R, que, por sua vez, emite duas partículas beta, transformado-se num elemento T, que emite uma partícula alfa, transformando-se no elemento D.
Sendo assim, podemos afirmar que
a) M e R são isóbaros.
b) M e T são isótonos.
c) R e D são isótopos.
d) M e D são isótopos.
e) R e T são isótonos.
31) (UFPE) A Coréia do Norte realizou, recentemente, um teste nuclear subterrâneo, que foi condenado pelo Conselho de Segurança da ONU. Sabe-se que as armas em desenvolvimento por aquele país estão baseadas em plutônio. O plutônio, entretanto, não é capaz de iniciar por si próprio uma reação em cadeia e, por isso, é utilizado juntamente com berílio e polônio. Considerando que o berílio tem Z=4 e A=9; o polônio tem Z=84 e A=209 ou 210 e o plutônio tem Z=94 e A=238, 239, 240, 241, 242 ou 244, analise as proposições a seguir.
00. O decaimento de Po-210 a  resulta na emissão de partículas alfa.
resulta na emissão de partículas alfa.
01. Se ocorrer um choque entre uma partículas alfa e o Be, ocorrerá formação de carbono-14 (radioativo) e emissão de 1 nêutron.
02. O Plutônio possui 6 isótopos.
03. Sabendo que o Pu-244 decai com emissão de partículas alfa de formação de U-240, com tempo de meia-vida de 80.000.000 anos, conclui-se que um átomo de urânio tem 92 prótons.
04. Uma vez que o Pu-238 pode ser formado a partir da emissão de uma partícula beta pelo netúnio (Np), concluímos que este elemento deve ter um isótopo com Z=95 e A=238.
32) (Unimontes MG) O núcleo de tório,  , ao sofrer desintegração radiativa, emite as seguintes partículas sucessivamente:
, ao sofrer desintegração radiativa, emite as seguintes partículas sucessivamente:  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  . Sabendo-se que uma partícula alfa e uma partícula beta são representadas por
. Sabendo-se que uma partícula alfa e uma partícula beta são representadas por  e
e  , após a desintegração, o nuclídeo estável formado é
, após a desintegração, o nuclídeo estável formado é
a)  b)
b)  c)
c)  d)
d) 
33) (UFSCAR SP) Físicos da Califórnia relataram em 1999 que, por uma fração de segundo, haviam produzido o elemento mais pesado já obtido, com número atômico 118. Em 2001, eles comunicaram, por meio de uma nota a uma revista científica, que tudo não havia passado de um engano.
Esse novo elemento teria sido obtido pela fusão nuclear de núcleos de 86Kr e 208Pb, com a liberação de uma partícula. O número de nêutrons desse "novo elemento" e a partícula emitida após a fusão seriam, respectivamente,
a) 175, nêutron. b) 175, próton. c) 176, beta. d) 176, nêutron. e) 176, próton.
34) (FCChagas BA) Um grama de 92U235 libera, ao sofrer fissão nuclear, aproximadamente 2 . 107kcal. Para saber quantos kcal são liberados na fissão de 1 mol de átomos desse isótopos, efetua–se o cálculo:
a) (2 . 107kcal/g) . 92g
b) (2 . 107kcal/g) . 235g
c) (2 . 107kcal/g) . (235 – 92)g
d) (2 . 107kcal/g) . (235 + 92)g
e) (2 . 107kcal/g) . (235 / 92)g
35) O decaimento de isótopos radioativos pode ser usado para medir a idade de fósseis. A equação que rege o processo é a seguinte:
N = N0 e-λt
sendo N0 > 0 o número inicial de núcleos radioativos, N o número de núcleos radioativos no tempo t e λ > 0 a taxa de decaimento. O intervalo de tempo necessário para que o número de núcleos radioativos seja reduzido à metade é denominado tempo de meia-vida. Pode-se afirmar que o tempo de meia-vida:
A) é igual a ln(2)/λ
B) é igual a 1/2
C) é igual a 2
D) é igual a -ln(2)/λ
E) depende de N0
36) (UNICAMP SP) A matéria orgânica viva contém uma relação 14C/12C constante. Com a morte do ser vivo, essa razão vai se alterando exponencialmente com o tempo, apresentando uma meia-vida de 5600 anos. Constatou-se que um riacho, onde ocorreu uma grande mortandade de peixes, apresentava uma quantidade anômala de substâncias orgânicas. Uma amostra da água foi retirada para análise. Estudando-se os resultados analíticos referentes à relação 14C/12C, concluiu-se que a poluição estava sendo provocada por uma indústria petroquímica e não pela decomposição natural de animais ou plantas que tivessem morrido recentemente.
a) Como foi possível, com a determinação da relação 14C/12C, afirmar com segurança que o problema tinha se originado na indústria petroquímica?
b) Descreva, em poucas palavras, duas formas pelas quais a presença dessa matéria orgânica poderia ter provocado a mortandade de peixes.
37) (UNICAMP SP) Existem várias hipóteses quanto à origem da Terra e sobre os acontecimentos que geraram as condições físico-químico-biológicas dos dias de hoje. Acredita-se que o nosso planeta tenha se formado há cerca de 4550 milhões de anos. Um dos estágios, logo no início, deve ter sido o seu aquecimento, principalmente pela radioatividade. A figura mostra a produção de energia a partir de espécies radioativas e suas abundâncias conhecidas na Terra.

a) Quantas vezes a produção de energia radiogênica (radioativa) era maior na época inicial de formação da Terra, em relação aos dias atuais?
b) Quais foram os dois principais elementos responsáveis pela produção de energia radiogênica na época inicial de formação da Terra?
c) E nos dias de hoje, quais são os dois principais elementos responsáveis pela produção dessa energia?
38) (FUVEST SP) Em 1999, a região de Kosovo, nos Bálcãs, foi bombardeada com projéteis de Urânio empobrecido, o que gerou receio de contaminação radioativa do solo, do ar e da água, pois urânio emite partículas alfa.
a) O que deve ter sido extraído do urânio natural, para se obter o urânio empobrecido? Para que se usa o componente retirado?
b) Qual a equação da primeira desintegração nuclear do urânio-238? Escreva-a, identificando o nuclídeo formado.
c) Quantas partículas alfa emite, por segundo, aproximadamente, um projétil de urânio empobrecido de massa 1 kg?
Dados: composição do urânio natural........................ U-238 - 99,3%
U-235 - 0,7%
meia-vida do U-238 ....................................... 5 x 109 anos
constante de Avogadro.................................. 6 x 1023 mol-1
1 ano ............................................................ 3 x 107s
alguns elementos e respectivos números atômicos
39) (FEPECS DF) “No coração das estrelas ocorre a fusão do hidrogênio em outros elementos. As enormes pressões geram temperaturas de dezenas de milhares de graus, que causam reações capazes de fundir prótons com prótons, formando, como num jogo de lego, outros elementos. Nas estrelas como o Sol, a fusão vai até o carbono e oxigênio. Nas mais pesadas, até o ferro. São elas as fornalhas alquímicas do cosmo.”
ALQUIMIA CÓSMICA, Marcelo Gleiser Folha de São Paulo, Caderno Mais, 18/09/2005.
Segundo o texto um elemento que NÃO devemos encontrar no Sol é o:
a) hélio; b) nitrogênio; c) boro; d) cloro; e) lítio.
40) (ITA 2009) O acidente nuclear ocorrido em Chernobyl (Ucrânia), em abril de 1986, provocou a emissão radioativa predominantemente de Iodo-131 e Césio-137. Assinale a opção CORRETA que melhor apresenta os respectivos períodos de tempo para que a radioatividade provocada por esses dois elementos radioativos decaia para 1% dos seus respectivos valores iniciais. Considere o tempo de meia-vida do Iodo-131 igual a 8,1 dias e do Césio-137 igual a 30 anos. Dados: 1n 100 = 4,6; 1n 2 = 0,69.
a) 45 dias e 189 anos.
b) 54 dias e 201 anos.
c) 61 dias e 235 anos.
d) 68 dias e 274 anos.
e) 74 dias e 296 anos.
a) 45 dias e 189 anos.
b) 54 dias e 201 anos.
c) 61 dias e 235 anos.
d) 68 dias e 274 anos.
e) 74 dias e 296 anos.
41) (UFPE) O programa nuclear do Irã tem chamado a atenção internacional em função das possíveis aplicações militares decorrentes do enriquecimento de urânio. Na natureza, o urânio ocorre em duas formas isotópicas, o U-235 e o U-238, cujas abundâncias são, respectivamente, 0,7% e 99,3%. O U-238 é radioativo, com tempo de meia-vida de 4,5 x 109anos. Independentemente do tipo de aplicação desejada. Sobre o uso do urânio, considere a equação abaixo e analise as afirmativas a seguir.
1. O U-238 possui três prótons a mais que o U-235.
2. Os três nêutrons liberados podem iniciar um processo de reação em cadeia.
3. O criptônio formado tem número atômico igual a 36 e número de massa igual a 96.
4. a equação acima representa a fissão nuclear do urânio.
5. devido ao tempo de meia-vida extremamente longo, o U-238 não pode, de forma alguma, ser descartado no meio ambiente.
Estão corretas apenas:
a) 1, 2 e 5 b) 2, 3, 4 e 5 c) 1, 3 e 4 d) 2, 4 e 5 e) 3, 4 e 5
42) (UNIFOR CE) Atualmente, a tomografia por Emissão de Pósitrons (PET) é muito utilizada em diagnóstico médico. A PET opera pela emissão de pósitrons por certos núcleos instáveis (tais como 11C, 15O, 18F) que, por colisões com elétrons, produzem raios gama.
próton (p+)  nêutron (nº) + pósitron (ºe+)
nêutron (nº) + pósitron (ºe+)
pósitron (ºe+) + elétron (ºe–) 
 (raio gama)
(raio gama)
Sendo assim, quando o núcleo do átomo de flúor,  , sofre essa transformação emitindo um pósitron, forma-se um átomo do elemento com número atômico
, sofre essa transformação emitindo um pósitron, forma-se um átomo do elemento com número atômico
a) 19 b) 17 c) 10 d) 9 e) 8
43) (UFG GO) Uma fonte radioativa, como o césio 137, que resultou num acidente em Goiânia, em 1987, é prejudicial à saúde humana porque
a) a intensidade da energia emitida não depende da distância do organismo à fonte.
b) a energia eletromagnética liberada pela fonte radioativa interage com as células, rompendo ligações químicas.
c) o sal solúvel desse elemento apresenta alta pressão de vapor, causando danos ao organismo.
d) a energia liberada violentamente sobre o organismo decorre do tempo de meia-vida, que é de alguns segundos.
e) a radiação eletromagnética liberada permanece no organismo por um período de meia-vida completo.
44) (UEMT) A reação nuclear 1H1 + 1H3 2He4 desenvolve uma quantidade fabulosa de energia, ou seja, da ordem de 5 . 108kcal para cada mol de He formado, havendo necessariamente uma variação de massa do sistema. Esta variação de massa poderá ser calculada através da:
a) lei de Coulomb b) lei de faraday c) lei de Lavoisier
d) equação de Planck e) equação de Eistein
45) (UEG GO) Radioatividade é o fenômeno pelo qual um núcleo instável emite espontaneamente determinadas partículas e ondas, transformando-se em outro núcleo mais estável.
As partículas e ondas emitidas pelo núcleo recebem genericamente o nome de radiações.
O fenômeno da radioatividade é exclusivamente nuclear, isto é, ele se deve unicamente ao núcleo do átomo.
Um átomo Y, de número atômico 88 e número de massa 226, emite duas partículas alfa, transformando-se num átomo X, o qual emite uma partícula beta, produzindo um átomo W.
Considerando essas informações, faça o que se pede:
a) Determine Z e A do átomo X.
b) Determine Z e A do átomo W.
46) (UFTM MG) A terapia para tratamento de câncer utiliza-se da radiação para destruir células malignas. O boro-10, não radioativo, é incorporado a um composto que é absorvido preferencialmente pelos tumores. O paciente é exposto a breves períodos de bombardeamento por nêutrons. Quando bombardeado, o boro-10 decai gerando partículas alfa, cuja radiação destrói as células cancerosas. Assim que o bombardeamento é interrompido, cessa a emissão dessas partículas. No bombardeamento com nêutrons, o boro-10 decai para o nuclídeo, que é um dos isótopos do:
a) nitrogênio. b) sódio. c) berílio. d) lítio. e) neônio.
47) (UERJ) O reator atômico instalado no município de Angra dos Reis é do tipo PWR - Reator de Água Pressurizada. O seu princípio básico consiste em obter energia através do fenômeno “fissão nuclear”, em que ocorre a ruptura de núcleos pesados em outros mais leves, liberando grande quantidade de energia. Esse fenômeno pode ser representado pela seguinte equação nuclear: 
Os números atômicos e de massa do elemento T estão respectivamente indicados na seguinte alternativa:
a) 27 e 91 b) 37 e 90 c) 39 e 92 d) 43 e 93
48) (UERJ) A meia-vida é o parâmetro que indica o tempo necessário para que a massa de uma certa quantidade de radioisótopos se reduza à metade de seu valor.
Considere uma amostra de 53I133, produzido no acidente nuclear, com massa igual a 2 g e meia-vida de 20 h.
Após 100 horas, a massa dessa amostra, em miligramas, será cerca de:
Após 100 horas, a massa dessa amostra, em miligramas, será cerca de:
(A) 62,5
(B) 125
(C) 250
(D) 500
49) (UFRRJ) Para determinar a constante de Avogadro, Rutherford observou a seguinte série radioativa:
A partir desta série, responda:
a) Qual será a relação entre o número de partículas  e partículas
e partículas  emitidas na série radioativa acima? Justifique.
emitidas na série radioativa acima? Justifique.
b) Sabendo que a meia vida do Polônio-218 é de 3,1 minutos, calcule o tempo que uma amostra leva para desintegrar 87,5% de sua massa.
50) (UFPR) O polônio-210 é um emissor alfa com um tempo de meia-vida de 138 dias. Supondo que se coloquem, em um recipiente fechado, 21g desse isótopo, ficando retidas, no recipiente, as partículas alfas que capturarão elétrons, transformando-se em hélio, teremos, ao fim de 276 dias, uma massa de hélio igual a (He-4):
a) 0,10g b) 0,20g c) 0,35g d) 0,30g e) 0,40g
51) Após 12 dias, uma substância radioativa tem a sua atividade reduzida para 1/8 da inicial. A meia-vida dessa substância será de:
- 3 dias.
- 4 dias.
- 6 dias.
- 8 dias.
- 12 dias.
52) O criptônio-89 possui o tempo de meia-vida igual a 3,16 minutos. Dispondo-se de uma amostra contendo 4,0 . 1023 átomos desse isótopo, ao fim de quanto tempo restarão 1,0 . 1023 átomos?
- 3,16 minutos
- 6,32 minutos
- 9,48 minutos
- 12,64 minutos
- 15,8 minutos
53) (FESP-SP) Bomba de cobalto é um aparelho muito usado na radioterapia para tratamento de pacientes, especialmente portadores de câncer. O material radioativo usado nesse aparelho é o 2760Co, com um período de meia-vida de aproximadamente 5 anos.
Admita que a bomba de cobalto foi danificada e o material radioativo exposto à população. Após 25 anos, a atividade deste elemento ainda se faz sentir num percentual, em relação à massa inicial, de:
a) 3,125% b) 6% c) 0,31% d) 31,25% e) 60%
54) A meia-vida de um isótopo radioativo é de 2 dias, partindo de 512g, que massa restará após 2 meses?
55) (ITA 2009) Considere duas reações químicas (I e II) envolvendo um reagente X. A primeira (I) é de primeira ordem em relação a X e tem tempo de meia-vida igual a 50 s. A segunda (II) é de segunda ordem em relação a X e tem tempo de meia-vida igual à metade da primeira reação. Considere que a concentração inicial de X nas duas reações é igual a 1,00 mol L-1. Em um gráfico de concentração de X (mol L-1) versus tempo (de 0 até 200 s), em escala, trace as curvas de consumo de X para as duas reações. Indique com I a curva que representa a reação de primeira ordem e, com II, a que representa a reação de segunda ordem.
56) A energia lançada no espaço pelo Sol:
a) provém das reações nucleares que ocorrem em seu interior por causa da alta pressão e da temperatura.
b) ocorrem na superfície.
c) ocorrem na fotosfera.
d) ocorrem na cromosfera.
e) não ocorrem no Sol.
57) (UFU-MG) Leia com atenção o texto abaixo e responda a questão proposta.
Quando o físico francês Antoine Henri Becquerel descobriu, em 1896, que o urânio emitia espontaneamente uma radiação que ele denominou “raios urânicos”, seguiu-se uma grande revolução no conhecimento científico. Sua descoberta contribuiu para a hipótese de que o átomo não era o constituinte último da matéria e abriu caminho para a área da física nuclear. O próprio Becquerel identificou que os “raios urânicos” eram constituídos de três partes distintas. Mais tarde, essas partes foram denominadas radiação alfa (núcleo do átomo de hélio), radiação beta (elétrons altamente energéticos) e radiação gama (de natureza eletromagnética). Marie Curie e seu marido Pierre Curie verificaram esse mesmo fenômeno em dois novos elementos, rádio e polônio, por eles descobertos.
Podemos afirmar que o texto:
a) trata da descoberta da radioatividade.
b) trata da descoberta do efeito fotoelétrico.
c) mostra a origem da radiação eletromagnética.
d) apresenta a origem do conceito de átomo.
e) n.d.a
58) Calcule a energia nuclear liberada numa reação em cadeia de um mol de átomos de urânio (dado: 1 mol = 6 x 1023 átomos).
a) 2,2 x 1012 J
b) 3,8 x 1014 J
c) 1,92 x 1013 J
d) 5,47 x 1011J
e) 1,6 x 1019 J
59) (INATEL) Os grandes reatores atômicos, atualmenteem uso, liberam energia de decorrência de:
a) Fissão nuclear. b) Fusão nuclear. c) Radioatividade natural.
d) Reações químicas do urânio 235. e) NRA.
I. Na usina térmica, o calor gerado pela combustão do carvão, do óleo ou do gás vaporiza a água em uma caldeira. Esse vapor aciona uma turbina acoplada a um gerador e este produz eletricidade.
II. O processo de fusão nuclear utilizado em algumas usinas nucleares é semelhante ao processo da fissão nuclear. A diferença entre os dois está na elevada temperatura para fundir o átomo de Urânio-235.
III. Na usina nuclear, o calor é produzido pela fissão do átomo do Urânio-235 por um nêutron no núcleo do reator.
IV. Na usina nuclear, o calor é produzido pela reação em cadeia da fusão do átomo do Urânio-235 com um nêutron.
São corretas apenas as afirmativas:
a) I e III. b) II, III e IV. c) I, II e IV. d) II e III. e) III e IV.
61) (UFG-GO) O sol fornece energia ao nosso planeta devido à fusão nuclear – a união de átomos de hidrogênio para formar hélio. Um exemplo de reação de fusão é a união de dois núcleos de deutério para dar um núcleo de hélio, um nêutron e energia, que pode ser representada como:
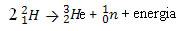
62) Para ser utilizado em reatores nucleares de fusão, o trítio pode ser produzido em escala industrial por meio do seguinte processo:
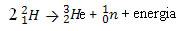
Sobre esse processo, é correto afirmar:
01. É uma reação química onde os reagentes são átomos de hidrogênio e os produtos são nêutrons, átomos de hélio e energia.
02. O deutério é um dos isótopos conhecidos do hidrogênio.
04. O hélio produzido é isóbaro do trítio, outro isótopo conhecido do hidrogênio.
08. O hidrogênio, o deutério e o trítio apresentam cargas nucleares diferentes.
16. Gases nobres podem ser produzidos por processos naturais.
32. Os números sobrescritos e subscritos correspondem, respectivamente, ao número de massa e ao número atômico.
02. O deutério é um dos isótopos conhecidos do hidrogênio.
04. O hélio produzido é isóbaro do trítio, outro isótopo conhecido do hidrogênio.
08. O hidrogênio, o deutério e o trítio apresentam cargas nucleares diferentes.
16. Gases nobres podem ser produzidos por processos naturais.
32. Os números sobrescritos e subscritos correspondem, respectivamente, ao número de massa e ao número atômico.
62) Para ser utilizado em reatores nucleares de fusão, o trítio pode ser produzido em escala industrial por meio do seguinte processo:
36Li + 01n → 13H + X
Uma possível reação nuclear de fusão pode ser dada pela equação:
Deutério + trítio → nêutron + Y
X e Y nas equações nucleares acima são:
- 24α. e -10β.
- 01n e 13H.
- 12H e 24He.
- 24He e 24He.
- 01n e 24He.
63) (UFMA) A bomba de hidrogênio funciona de acordo com a seguinte reação nuclear:
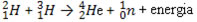
- é reação de “fusão”.
- é reação de “fissão”.
- é reação onde ocorre apenas emissão de partículas 24α.
- é reação onde ocorre apenas emissão de partículas -10β.
- é reação onde ocorre apenas emissão de raios 00γ.
64) (puc-rj) Uma das características das últimas décadas foram as crises energéticas. Neste contexto, tivemos várias notícias nos jornais relacionadas com diferentes formas de geração de energia. As afirmativas abaixo poderiam ter constado de algumas dessas matérias:
I - O reator nuclear Angra II, que entrou em operação este ano, gera energia através da fusão nuclear de átomos de urânio enriquecido.
II - A queima de combustível fóssil, por exemplo a gasolina, constitui-se, na realidade, numa reação de oxidação de matéria orgânica.
III - A queima de uma dada quantidade de carvão em uma termoelétrica produz a mesma quantidade de energia que a fissão de igual massa de urânio em uma usina nuclear.
IV - É possível aproveitar a energia solar utilizando-se a eletrólise da água durante o dia e queimando-se o hidrogênio produzido durante a noite.
II - A queima de combustível fóssil, por exemplo a gasolina, constitui-se, na realidade, numa reação de oxidação de matéria orgânica.
III - A queima de uma dada quantidade de carvão em uma termoelétrica produz a mesma quantidade de energia que a fissão de igual massa de urânio em uma usina nuclear.
IV - É possível aproveitar a energia solar utilizando-se a eletrólise da água durante o dia e queimando-se o hidrogênio produzido durante a noite.
Dentre as afirmações acima, apenas está(ão) correta(s):
(A) I. (B) III. (C) I e II. (D) II e IV. (E) III e IV.
65) (PUC-SP) Na sequência radioativa:84216A → 82212B → 83212C → 84212D → 82208E
temos, sucessivamente, emissões:- -10β -10β -10β 24α
- 24α -10β -10β 24α
- 24α -10β 24α -10β
- 24α 24α -10β -10β
- -10β 24α 24α -10β
66) (UFPE) O núcleo atômico de alguns elementos é bastante instável e sofre processos radioativos para remover sua instabilidade. Sobre os três tipos de radiação α, β e γ, podemos dizer que:
68) O radioisótopo 222 do 86Rn, por uma série de desintegrações, transforma-se no isótopo 206 do 82Pb. Determine o número de partículas alfa e o número de partículas beta envolvidas nessas transformações.
Gabarito:
0. ao emitir radiação α, um núcleo tem seu número de massa aumentado.
1. ao emitir radiação β, um núcleo tem seu número de massa inalterado.
2. a radiação α é constituída por núcleos de átomos de hélio.
3. ao emitir radiação γ, um núcleo não sofre alteração em sua massa.
4. ao emitir radiação β, um núcleo tem seu número atômico aumentado em uma unidade.
67) O elemento netúnio (93237Np), após a emissão de sete partículas alfa e quatro partículas beta, transforma-se em qual elemento químico?
- 92238U
- 90232Th
- 88226Ra
- 85210At
- 83209Bi
- 2 partículas alfa e 2 partículas beta
- 2 partículas alfa e 4 partículas beta
- 4 partículas alfa e 3 partículas beta
- 4 partículas alfa e 4 partículas beta
- 3 partículas alfa e 3 partículas beta
1) A 2) D 3) C 4) E 5) D 6) D 7) B
8) A equação que representa o fenômeno é: 7N14 + 0n1 - 6C14 + bya
Cálculo de a: 14 + 1 = 14 + a \ a = 1Cálculo de b: 7 + 0 = 6 + b \ b = 1
1y1 = 1p1 (próton)
A equação completa é: 7N14 + 0n1 - 6C14 + 1p1
9) E 10) 11 11) B 12) A
13) Inicialmente, é preciso calcular a variação do número de massa na etapa III, que corresponde à diferença entre os números de massa dos átomos participantes:
234 - 210 = 24
Cada partícula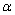 apresenta número de massa igual a 4. Logo, o número de partículas
apresenta número de massa igual a 4. Logo, o número de partículas 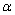 emitidas equivale a:
emitidas equivale a:
24 : 4 = 6
Nesta mesma etapa, a variação do número atômico é dada por:
91 - 84 = 7
As partículas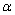 e ß apresentam número atômico igual a 2 e -1, respectivamente. Considerando y o número de partículas ß, tem-se:
e ß apresentam número atômico igual a 2 e -1, respectivamente. Considerando y o número de partículas ß, tem-se:
Cada partícula
24 : 4 = 6
Nesta mesma etapa, a variação do número atômico é dada por:
91 - 84 = 7
As partículas
6 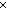 2 = 7
2 = 7
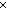 2 = 7
2 = 7
y = 5
Na etapa III, portanto, são emitidas 6 partículas 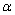 e 5 partículas ß.
e 5 partículas ß.
Átomos isóbaros são aqueles que apresentam o mesmo número de massa. Na sequência apresentada, Th e Pa são isóbaros, pois ambos apresentam número de massa igual a 234.
14) Questão simples de radioatividade, mais especificamente abordando emissões de partículas. A emissão pode ser representada como segue:
Resposta: C
15) Nosso objetivo inicial é determinar quantos átomos de trítio existiam na amostra de 10 g da água do rio.
18 g água ___________ 6.10²³ moléculas água
10g água ___________ x
x = 3,3.10²³ moléculas de água.
Como cada molécula de água possui 2 átomos de hidrogênio, no total teremos 6,6.10²³ átomos de hidrogênio na amostra.
Foi nos dito que:
8.10-18 átomos de trítio __________ 1 átomo de hidrogênio
y __________ 6,6.10²³ átomos de hidrogênio
y = 5,28.106 átomos de trítio
Sabemos que, do decaimento radioativo do trítio teremos:
N = N0/2t, onde t é o número de meias-vidas que se passaram.
No nosso caso temos:
1 meia-vida __________ 12,26 anos
t __________ 40 anos
t = 3,26 meias-vidas
Portanto:
N = 5,28.106/23,26
N = 5,5.105 átomos de trítio
16) O enunciado nos diz que, no principio da Terra as quantidades de U-235 e U-238 eram iguais, uma vez que não exisitiria motivo aparente para formação preferencial de qualquer um dos dois.
Suponha que as massas iniciais eram iguais a M.
Após todo o tempo passado da existência terrestre, a proporção dos isótopos mudou. Isso fica claro quando vemos que o tempo de meia-vida do U-235 é menor que o do U-238 ou seja, o U-235 se desintegra mais rápido que o U-238.
Para determinar as massas atuais dos dois isótopos vamos usar que:
m = M/2x, onde x corresponde ao número de meias-vidas que já se passaram para cada um dos isótopos, de modo que x pode ser representado por:
x = T/t1/2, sendo t1/2 o tempo de meia-vida do isótopo radioativo.
• U-235
m = M/2x → aplicando log dos dois lados
x.log2 = log (M/m235)…(I)
• U-238
m = M/2y → aplicando log dos dois lados
y.log2 = log(M/m238)…(II)
Fazendo (I) − (II) teremos:
(x – y).log2 = log(m238/m235)
Foi nos dada a relação de porcentagem mássica entre U-235 e U-238 ,logo:
m238/m235 = 99,28/0,72 = 137,89
Com isso, log(m238/m235) = 2,14
Das definições apresentadas sobre as expressões de x e y temos:
x – y = T.(1/7,07 .108 − 1/4,50 .109)
x – y = (45 – 7,07).T/318,15.108
x – y = 0,12T/108
Como log2 = 0,3 teremos:
(0,12 x 0,3)T/108 = 2,14
T = 5,4.109 anos
17) Veja que:
210Po → 206Pb + 4α
Em contato com o ar, as partículas α irão abstrair elétrons se tornando átomos de He.
Considerando que em 1 ano temos 365 dias, o número de meias-vidas que terão se passado foi de:
x = 365/138,4 = 2,64
Em posse dessa informação podemos calcular qual a massa remanescente de Po-210 na amostra.
m = m0/2x
m = 1/6,22 = 0,16g
Com isso, podemos descobrir de forma simples qual a massa de Po-210 que se transformou em hélio. Afinal:
mreagiu = minicial – mrestou
mreagiu = 1 – 0,16 = 0,84 g
Como 1 mol de Po-210 emitem 1 mol de partículas-alfa teremos:
1 mol Po-210 ___________ 1 mol He
210g Po-210 ___________ 22,4 L He
0,84 g Po-210 __________ V
V = 0,0896 L → V = 89,6 mL
18) O processo radioativo é dado por:
11Na → 12Mg + -1β
Como a relação mássica entre os isótopos de Mg e Na deve ser de 1:3, se a massa de Mg for m, a massa de Na será 3m.
Sabemos que, no decaimento β a conversão de massa em energia é muito pequena, logo a massa total se mantém praticamente inalterada com o passar do tempo.
Isso nos mostra que: 3m + m = 200
m = 50 mg
Logo, após um tempo Δt, da massa inical de 200 mg de Na-24 restarão apenas 150 mg.
Sabemos que: m =m0/2x, onde x é igual ao número de meias-vidas que se passaram.
150 = 200/2x
2x = 4/3. (aplicando log dos dois lados da equação)
xlog2 = log4 – log3
0,3x = 0,6 – 0,47
x = 0,4333…
O número de meias-vidas pode ser calculado ainda da seguinda forma:
x = Δt/T, onde T é o tempo de meia-vida.
0,4333… = Δt/15
Δt = 6,5 h = 6 horas e 30 minutos
19) Após 7,6 dias já terão se passado duas meias-vidas. Ou seja, a quantidade de rádio será 1/4 da original.
Isso nos permite ver que 0,75 mol de rádio-226 decaíram transformando-se em He-4 e radônio-222.
Da reação temos: 226Ra → 222Rn + 4He
Como a proporção de rádio-226 consumido para hélio-4 e radônio-222 formados é de 1:1, após 7,6 dias teremos 0,75 mol de He e 0,75 mol de Rn na ampola.
Como os dois gases não reagem entre si. o número de mols total de gás adicional na ampola será de 1,5.
Usando a equação dos gases ideais: pV = nRT
p = (1,5 x 0,082 x 300)/8,2
p = 4,5 atm.
Como a pressão inicial na ampola já era de 1,5 atm concluímos que a pressão final é:
pf =4,5 + 1,5
pf = 6,0 atm
20) Vamos primeiramente determinar o número atômico de X.
Explicitando somente essa váriável teremos:
99Es + 2α → 2 0n + X
Como o número de prótons de ambos os lados do processo de desintegração tem que ser iguais teremos:
99 + 2 = (2 x 0) + px
px = 101
Analogamente ao processo citado anteriormente teremos, para a variável massa:
253Es + 4α → 2 1n + X
253 + 4 = 2 + Mx
Mx = 255
Portanto, os números atômico e de massa de X são respectivamente 101 e 255.
21) E 22) D 23) D
24) a) A semi-reação que ocorre no pólo negativo da cuba eletrolítica é:





24) a) A semi-reação que ocorre no pólo negativo da cuba eletrolítica é:
cátodo: 2D2O + 2e–  D2 + 2OD–2
D2 + 2OD–2
O deutério e o prótio são isótopos do hidrogênio, deste modo, ambos os núcleos possuem o mesmo número de prótons (Z) e diferem no número de nêutrons.

b) A reação de fusão nuclear descrita:
2
 +
+ 
As fusões nucleares conhecidas ocorrem em condições solares (temperatura e pressão muito elevadas), o que limita e muito as suas aplicações tecnológicas: uma fusão nuclear a frio (condições do ambiente) é muito importante porque eliminaria as limitações citadas.
25) 05
26) A resolução da questão exige apenas uma interpretação do gráfico. Como o fármaco foi injetado às 12h e tem uma meia-vida de 1h, o número de meias-vidas será de 1,5. Analisando o gráfico, concluímos que haverá cerca de 35% do fármaco no organismo.
Resposta: D
27) FVFVV 28) 02 29) F–V–F–V–V 30) C 31) VFVVF 32) C 33) A 34) B
26) A resolução da questão exige apenas uma interpretação do gráfico. Como o fármaco foi injetado às 12h e tem uma meia-vida de 1h, o número de meias-vidas será de 1,5. Analisando o gráfico, concluímos que haverá cerca de 35% do fármaco no organismo.
Resposta: D
27) FVFVV 28) 02 29) F–V–F–V–V 30) C 31) VFVVF 32) C 33) A 34) B
35) A
36) a) Caso a poluição estivesse sendo provocada pela decomposição natural de animais ou plantas mortos recentemente, a relação 14C/12C seria praticamente igual à de um ser vivo. Como matéria-prima a indústria petroquímica utiliza material fóssil, originado de organismos vivos que morreram há milhares de anos. Por isso, a poluição produzida pela indústria petroquímica apresentará uma relação 14C/12C menor que a de um ser vivo.
b) A decomposição da matéria orgânica que contamina o riacho consome o gás oxigênio dissolvido na água, fazendo com que os peixes morram por hipóxia (falta de oxigênio). O material orgânico também bloqueia a passagem de luz, impedindo que seja realizado o processo de fotossíntese pelos vegetais do riacho. Dessa forma, há uma menor produção de gás oxigênio e, conseqüentemente, uma menor oferta de O2 aos peixes.
37) a)

De acordo com o gráfico:
energia radiogênica na época inicial = 9,5
energia radiogênica após 4,55 bilhões de anos (hoje) 1,9
9,5/1,9 = 5,0. Assim, a produção de energia radiogênica era 5 vezes maior.
b) O elemento urânio, na forma do isótopo 235U, e o elemento potássio, na forma do isótopo 40K.
c) O elemento urânio, na forma do isótopo 238U, e o thório, na forma de isótopo 232Th.
38) a) Para obter urânio empobrecido, deve-se retirar, do urânio natural, o urânio 235.
O urânio 235 é utilizado em reatores de fissão nuclear e na bomba atômica.
b) 1 . 107 partículas
39) D 40) B 41) D 42) E 43) B 44) E 45) a) Z = 86; A = 222 b) Z = 87; A = 222
46) D 47) B
48) Alternativa A.
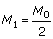
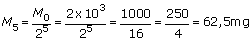
No instante inicial t0 = 0, a massa do radioisótopo é igual a M0 = 2 g = 2 x 103 mg.
Após um período de tempo igual a uma meia-vida, tem-se:
Após um período de tempo igual a uma meia-vida, tem-se:
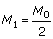
Após um período de duas meias-vidas:
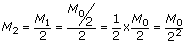
Observa-se, assim, que a massa diminui segundo uma P.G. de razão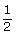 , cujo termo geral é dado por:
, cujo termo geral é dado por:
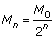
sendo n o número de meias-vidas.
Como a meia-vida do radioisótopo é igual a 20 h, para um período de tempo correspondente a 5 meias-vidas (100 h), a massa do radioisótopo será cerca de:
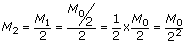
Observa-se, assim, que a massa diminui segundo uma P.G. de razão
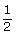 , cujo termo geral é dado por:
, cujo termo geral é dado por: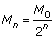
sendo n o número de meias-vidas.
Como a meia-vida do radioisótopo é igual a 20 h, para um período de tempo correspondente a 5 meias-vidas (100 h), a massa do radioisótopo será cerca de:
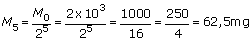
Percentual de acertos: 45,49%
49) a)
Como nesta série foram emitidas 4 partículas alfa e duas partículas beta, a razão será 4/2 = 2
b) t = 9,3 min
50) Alternativa ‘d’.
50) Alternativa ‘d’.
A massa inicial de polônio é de 21 g, e o seu número de mol é dado por:
__21g___ = 0,1 mol
210 g/mol
210 g/mol
0,1 mol de Po → após 138 dias → 0,05 mol de Pó → após 138 dias → 0,025 mol de Po
276 dias
276 dias
O número de mol de Po que se desintegrou é igual a 0,075 mol, que originou 0,075 mol de hélio.
1 mol de He -------- 4g
0,075 mol de He --- x
x = 0,30 g de He
0,075 mol de He --- x
x = 0,30 g de He
51) Alternativa “b”.
A atividade ou velocidade de desintegração é proporcional à massa. Assim, ao final de 12 dias, teremos:
minicial = minicial
8 2x
1 = 1
8 2x
1 = 1
23 2x
x = 3
Portanto, as meias-vidas transcorridas em 12 dias são 3. Para determinar a duração de cada meia-vida, aplicamos uma regra de três:
3 meias vidas --------- 12 dias
1 meia-vida ----------- y
y = 1 . 12 dias
3
y = 4 dias.
mfinal = 1 minicial
8
Abaixo temos a fórmula da expressão geral usada para calcular a massa (mfinal) existente após x meias-vidas:8
mfinal = minicial
2x
Assim, podemos escrever:2x
minicial = minicial
8 2x
1 = 1
8 2x
1 = 1
23 2x
x = 3
Portanto, as meias-vidas transcorridas em 12 dias são 3. Para determinar a duração de cada meia-vida, aplicamos uma regra de três:
3 meias vidas --------- 12 dias
1 meia-vida ----------- y
y = 1 . 12 dias
3
y = 4 dias.
52) Alternativa “b”.
53) Alternativa ‘a’.
m = 512/2^30
m = 512/1073741824
m = 0,00000047gramas
m = 47.10^-8 gramas
53) Alternativa ‘a’.
100% x → 5 anos → 50% x → 5 anos → 25% x → 5 anos → 12,5% x → 5 anos → 6,25% x → 5 anos → 3,125% x
5 . 5 = 25 anos.
54) Para calcularmos a massa final de um decaimento radioativo, temos:
m = mo/2^n (Massa final é igual a Massa inicial dividida por 2 elevado ao número de Meia-Vida)5 . 5 = 25 anos.
m = 512/2^30
m = 512/1073741824
m = 0,00000047gramas
m = 47.10^-8 gramas
55)

56) A energia liberada pelo Sol provém de reações nucleares que ocorrem no interior do Sol, pelo fato de a pressão e a temperatura serem altíssimas. As reações que ocorrem são de fusão de núcleos de átomos de hidrogênio que se transformam em átomos de hélio.
58) Lembrando que cada átomo de urânio que sofre fissão nuclear libera 3,2 x 10-11 J, então temos:
63) Alternativa “a”.
Portanto, alternativa A
57) De acordo com o texto, podemos identificar que o elemento químico estudado tanto por Becquerel quanto pela família Curie emitia radiações que inicialmente foram chamadas de raios urânicos.
Portanto, alternativa A.
58) Lembrando que cada átomo de urânio que sofre fissão nuclear libera 3,2 x 10-11 J, então temos:
E = 6 x 1023 x 3,2 x 10-11
E = 1,92 x 1013 J
59) A 60) A
61) 54. São corretos: 02,04,16 e 32.
E = 1,92 x 1013 J
59) A 60) A
61) 54. São corretos: 02,04,16 e 32.
01. Errado, pois não é uma reação química, mas sim uma reação nuclear.
08. Errado, pois o hidrogênio, o deutério e o trítio são isótopos, portanto apresentam a mesma carga nuclear (Z = 1).
62) Alternativa “d”.
As somas dos números de massas (A) e dos números atômicos (Z) devem ser iguais nos produtos e nos reagentes. Assim, temos:
- 36Li + 01n → 13H + 24X (24X = 24He)
- Deutério + trítio → nêutron + Y
12H + 13H → 01n + 24Y (24Y = 24He)
63) Alternativa “a”.
A bomba de hidrogênio é uma bomba de fusão, ou seja, em que dois átomos leves fundem-se para formar um único átomo mais pesado.
64) D) II e IV.
66)
0. Falsa. Ao emitir a radiação α, o núcleo tem o seu número de massa diminuído em 4 unidades porque essa emissão corresponde a um núcleo atômico de hélio, com 2 prótons e 2 nêutrons.
1. Verdadeira. A radiação β possui massa desprezível e sua emissão não provoca alteração no número de massa do nuclídeo.
2. Verdadeira.
3. Verdadeira. A emissão γ (gama) é pura radiação eletromagnética e não possui massa.
4. Verdadeira. A emissão β corresponde à perda de uma carga negativa por parte do núcleo, o que causa o aumento no número atômico em uma unidade.
67)
O número de massa diminui 16 unidades. Como cada radiação alfa significa uma diminuição no número de massa em 4 unidades, temos que foram emitidas 4 partículas alfa, pois 4 . 4 = 16. Nesse momento, significou que ele perdeu também 2 unidades no número atômico para cada partícula alfa, dando um total de 8 e ficando com o número atômico igual a 78 (86 – 8).
Para cada partícula beta emitida, o elemento ganha 1 unidade no número atômico. Como ele está com 78 e precisa atingir o número atômico igual a 82, ele emitiu 4 partículas beta.
Fontes: http://www.coladaweb.com/64) D) II e IV.
A afirmativa I está errada porque um reator utiliza a fissão e não a fusão nuclear.
A afirmativa III está errada porque a energia liberada numa fissão nuclear é milhões de vezes maior do que a energia liberada na queima (uma reação química) do carvão.
65) Alternativa “b”
84216A → 24α → 82212B → -10β → 83212C → -10β → 84212D → 24α →82208E66)
0. Falsa. Ao emitir a radiação α, o núcleo tem o seu número de massa diminuído em 4 unidades porque essa emissão corresponde a um núcleo atômico de hélio, com 2 prótons e 2 nêutrons.
1. Verdadeira. A radiação β possui massa desprezível e sua emissão não provoca alteração no número de massa do nuclídeo.
2. Verdadeira.
3. Verdadeira. A emissão γ (gama) é pura radiação eletromagnética e não possui massa.
4. Verdadeira. A emissão β corresponde à perda de uma carga negativa por parte do núcleo, o que causa o aumento no número atômico em uma unidade.
67)
Alternativa “e”.
Quando o elemento emite uma partícula alfa, ele perde dois prótons e dois nêutrons, isso significa que ele se transforma em um elemento com o número de massa (A = P + N) menor 4 unidades e o número atômico (Z = P ) menor duas unidades. Quando o elemento emite uma partícula beta, ele perde um elétron. Assim, temos:
93237Np → 7 24α +4 -10β + ZAX
A:
237 = 7 . 4 + 4 . 0 + A
A = 237 – 28
A = 209
Z:
93 = 7 . 2 + 4 . (-1) + Z
Z = 93 – 10
Z = 83
Assim, o elemento obtido é o 83209Bi.
68) Alternativa “d”.
86222Rn → 82206PbQuando o elemento emite uma partícula alfa, ele perde dois prótons e dois nêutrons, isso significa que ele se transforma em um elemento com o número de massa (A = P + N) menor 4 unidades e o número atômico (Z = P ) menor duas unidades. Quando o elemento emite uma partícula beta, ele perde um elétron. Assim, temos:
93237Np → 7 24α +4 -10β + ZAX
A:
237 = 7 . 4 + 4 . 0 + A
A = 237 – 28
A = 209
Z:
93 = 7 . 2 + 4 . (-1) + Z
Z = 93 – 10
Z = 83
Assim, o elemento obtido é o 83209Bi.
68) Alternativa “d”.
O número de massa diminui 16 unidades. Como cada radiação alfa significa uma diminuição no número de massa em 4 unidades, temos que foram emitidas 4 partículas alfa, pois 4 . 4 = 16. Nesse momento, significou que ele perdeu também 2 unidades no número atômico para cada partícula alfa, dando um total de 8 e ficando com o número atômico igual a 78 (86 – 8).
Para cada partícula beta emitida, o elemento ganha 1 unidade no número atômico. Como ele está com 78 e precisa atingir o número atômico igual a 82, ele emitiu 4 partículas beta.
http://alunoarretado.wordpress.com/
http://equipesolucao.wordpress.com/
http://exercicios.brasilescola.com/
http://exercicios.brasilescola.com/


Nenhum comentário:
Postar um comentário